- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Naposledy zmenené 2025-01-22 17:09.
Koncentráciu alebo objem koncentrovaného alebo zriedeného roztoku môžete vyriešiť pomocou rovnica : M1V1 = M2V2 , kde M1 je molárna koncentrácia (mol/litre) koncentrovaného roztoku, V2 je objem koncentrovaného roztoku, M2 je molarita zriedeného roztoku (po
Podobne sa môžete pýtať, prečo funguje m1v1 m2v2?
Mení sa len koncentrácia a mení sa objem. Počet mólov rozpustenej látky zostáva konštantný, pokiaľ nepridáte viac rozpustenej látky! Vzťah je teda založený na skutočnosti, že počet mólov rozpustenej látky zostane konštantný, ale koncentrácia a objem celého roztoku sa môžu meniť.
Následne je otázkou, ako používate vzorec n1v1 n2v2? N1V1 (HCl)= N2V2 (Na2CO3) alebo N1 × 10 = 0,2 × 25 ∴ N1 = 5 / 10 = 0,5 N Normálnosť × Ekvivalentná hmotnosť = Sila v gramoch na liter. 0,5 x 36,5 = 18,25. Sila roztoku HCl je 18,25 gramov na liter.
Okrem toho, aký je vzorec pre titráciu?
Použi titračný vzorec . Ak titrátor a analyt majú molárny pomer 1:1, vzorec je molarita (M) kyseliny x objem (V) kyseliny = molarita (M) zásady x objem (V) zásady. (Molarita je koncentrácia roztoku vyjadrená ako počet mólov rozpustenej látky na liter roztoku.)
Ako používate m1v1 m2v2?
Môžete vyriešiť koncentráciu alebo objem koncentrovaného alebo zriedeného roztoku použitím rovnica: M1V1 = M2V2 , kde M1 je molárna koncentrácia (mol/litre) koncentrovaného roztoku, V2 je objem koncentrovaného roztoku, M2 je molarita zriedeného roztoku (po
Odporúča:
Aký je vzorec pre pi kruhu?

Použite vzorec. Obvod kruhu sa zistí podľa vzorca C= π*d = 2*π*r. Pi sa teda rovná obvodu kruhu vydelenému jeho priemerom
Aký je empirický vzorec oktánového čísla?

C8H18 Aký je empirický vzorec oktánového čísla c8h18? The empirický vzorec oktánového čísla $$C_{8}H_{18}$$ je: A. B. C. Podobne, aký je empirický vzorec c2h6o2? Molekulárne a empirické vzorce Otázka Odpoveď Napíšte empirický vzorec pre nasledujúcu zlúčeninu:
Aký je vzorec Sin Cos Tan?
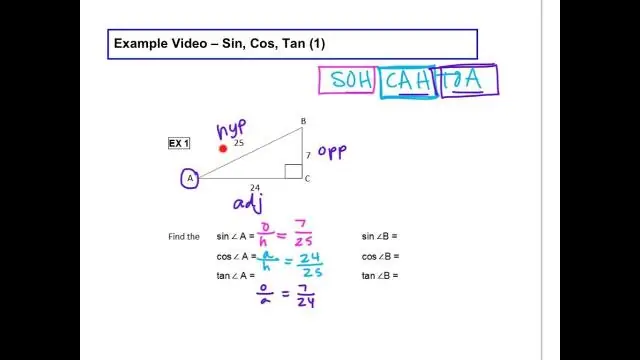
Funkcie sin, cos a tan možno vypočítať nasledovne: Funkcia sínus: sin(θ) = opak / prepona. CosineFunction: cos(θ) = sused / prepona. Funkcia dotyčnice: tan(θ) = Opačný /Susedný
Aký je empirický vzorec pre kofeín?
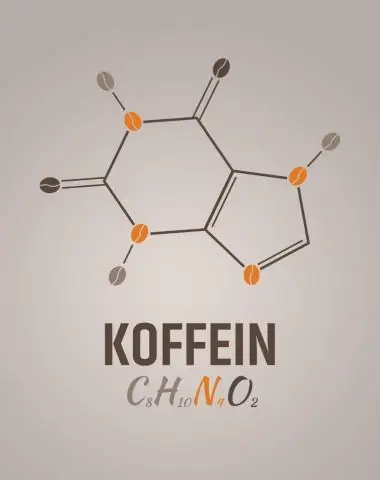
2 odpovede. C8H10N4O2 je molekulárny vzorec pre kofeín
Čo je empirický vzorec a molekulový vzorec?
Molekulárne vzorce vám povedia, koľko atómov každého prvku je v zlúčenine, a empirické vzorce vám povedia najjednoduchší alebo najviac znížený pomer prvkov v zlúčenine. Ak už nie je možné redukovať molekulový vzorec zlúčeniny, potom je empirický vzorec rovnaký ako molekulový vzorec
