
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:40.
- Naposledy zmenené 2025-01-22 17:09.
The Kvantové číslo uhlovej hybnosti ( l ) opisuje tvar orbitálu. The povolené hodnoty z l rozsah od 0 do n - 1. Magnet kvantové číslo (ml) opisuje orientáciu orbitálneho priestoru.
Podobne sa možno pýtať, čo určuje kvantové číslo momentu hybnosti?
The moment hybnosti kvantové číslo , ℓ, isthe kvantové číslo spojené s angularmomentum atómového elektrónu. The moment hybnosti kvantové číslo určuje tvar elektrónového sorbitalu.
Čo tiež určuje kvantové číslo? Riaditeľ kvantové číslo definuje všeobecnú veľkosť a energiu orbitálu. Hodnota l špecifikuje tvar orbitálu. Orbitály s rovnakou hodnotou l tvoria podplášť. Navyše, čím väčší je uhlový moment kvantové číslo , tým väčšia je moment hybnosti aneelektrónu na tomto orbitále.
Podobne sa môžete opýtať, aké sú možné hodnoty L?
Počet hodnoty orbitálneho uhlového čísla l možno použiť aj na identifikáciu počtu podobalov v hlavnom elektrónovom obale: Keď n = 1, l = 0( l nadobudne jednu hodnotu a teda môže existovať iba jedna podplášť) Keď n = 2, l = 0, 1 ( l berie na seba dvoch hodnoty a teda sú dve možné subshells)
Aký je vzorec azimutálneho kvantového čísla?
Moment hybnosti kvantové číslo , l, (označovaný aj ako sekundárny kvantové číslo alebo azimutálne kvantové číslo ) opisuje tvar orbitálu, ktorý aneelektrón zaberá. Najnižšia možná hodnota l je 0 a jej najvyššia možná hodnota v závislosti od istiny kvantové číslo , je n-1.
Odporúča:
Sú celé čísla vždy niekedy alebo nikdy racionálne čísla?

1,5 je racionálne číslo, ktoré možno zapísať ako: 3/2, kde 3 aj 2 sú celé čísla. Tu je racionálne číslo 8 celé číslo, ale racionálne číslo 1,5 nie je celé číslo, pretože 1,5 nie je celé číslo. Takže môžeme povedať, že racionálne číslo je celé číslo, niekedy nie vždy. Preto je niekedy správna odpoveď
Čo sú prirodzené čísla celé čísla, celé čísla a racionálne čísla?
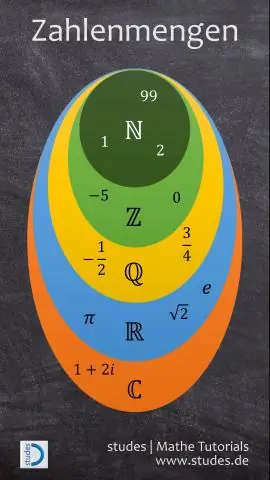
Reálne čísla sa delia hlavne na racionálne a iracionálne čísla. Racionálne čísla zahŕňajú všetky celé čísla a zlomky. Všetky záporné celé čísla a celé čísla tvoria množinu celých čísel. Celé čísla pozostávajú zo všetkých prirodzených čísel a nuly
Aký je príklad momentu hybnosti?

Príklady zachovania uhlovej hybnosti Predstavte si rotujúceho korčuliara. Ďalším populárnym príkladom zachovania momentu hybnosti je prípad osoby, ktorá drží rotujúce koleso bicykla na rotujúcej stoličke. Osoba potom prevráti koleso bicykla, čo spôsobí jeho otáčanie v opačnom smere, ako je znázornené nižšie
Aká je derivácia momentu hybnosti?

Kľúčové rovnice Rýchlosť ťažiska pohybujúceho sa objektu vCM=Rω Derivácia momentu hybnosti sa rovná krútiacemu momentu d→ldt=∑→τ Moment hybnosti sústavy častíc →L=→l1+→l2+⋯+→lN Pre sústavu častíc sa derivácia momentu hybnosti rovná krútiacemu momentu d→Ldt=∑→τ Moment hybnosti rotujúceho tuhého telesa L=Iω
Aké sú možné hodnoty L pre každú hodnotu n?

Subshells. Počet hodnôt orbitalulárneho čísla l možno použiť aj na identifikáciu počtu podplášťov v hlavnom elektrónovom obale: Keď n = 1, l= 0 (l nadobudne jednu hodnotu a teda môže existovať iba jedna podplášťovka) Keď n = 2 , l= 0, 1 (naberá dve hodnoty a teda existujú dve možné podvrstvy)
